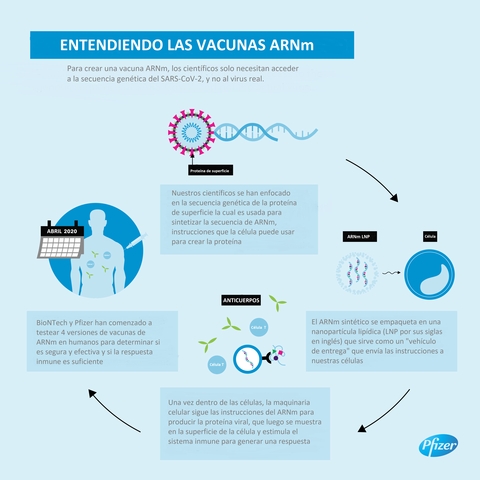
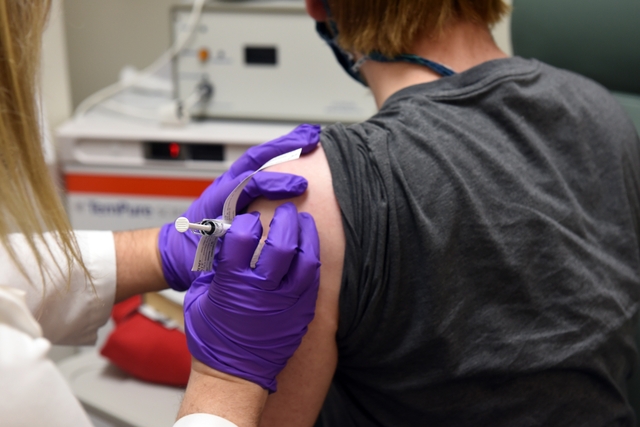
Pfizer Inc. y BioNTech SE anunciaron el inicio de un estudio clínico global (excepto en China) Fase 2/3 de seguridad y eficacia para evaluar a un candidato de ARN mensajero modificado con un único nucleósido (modARN) de su programa de vacunas basado en BNT162 ARNm contra SARS-CoV-2.
Después de una extensa revisión de los datos preclínicos y clínicos de los ensayos de Fase 1/2, y en colaboración con el Centro de Evaluación e Investigación Biológica (CBER) de la FDA, entre otros reguladores mundiales, Pfizer y BioNTech han optado por avanzar su candidato a la vacuna BNT162b2 en el estudio Fase 2/3, a un nivel de dosis de 30 μg en un régimen de 2 dosis. Dicho candidato de vacuna, que recientemente recibió la designación “Fast Track” de la FDA, codifica una glicoproteína de longitud completa (Proteína S) de SARS-CoV-2, convirtiéndola en el objetivo de los anticuerpos neutralizantes del virus.
«Nuestra selección del candidato a la vacuna BNT162b2 y su avance a un estudio de Fase 2/3 son la culminación de un programa de I+D amplio, colaborativo y sin precedentes en el que participaron Pfizer, BioNTech, investigadores clínicos y participantes del estudio, con el enfoque singular de desarrollar una vacuna ARN contra el COVID-19 segura y eficaz. El protocolo de estudio Fase 2/3 sigue todas las directrices de la Administración de Alimentos y Medicamentos de los Estados Unidos, respecto al diseño de ensayos clínicos para estudios de vacunas COVID-19», dijo Kathrin U. Jansen, Ph.D., Vicepresidenta Senior y Jefa de Investigación y Desarrollo de Vacunas en Pfizer. «El inicio del ensayo de Fase 2/3 es un gran
paso para nuestro progreso hacia el suministro de una vacuna potencial que ayude a combatir la pandemia COVID-19 en curso y esperamos generar datos adicionales a medida que el programa avance».
«Hoy, estamos comenzando nuestro estudio global en etapas tardías de la enfermedad, que incluirá hasta 30.000 participantes. Seleccionamos la BNT162b2 como nuestra candidata principal para esta prueba de Fase 2/3 tras una diligente evaluación de la totalidad de los datos generados hasta el momento. Esta decisión refleja nuestro objetivo principal de llevar una vacuna bien tolerada y altamente eficaz al mercado lo más rápido posible, mientras continuamos evaluando a nuestras otras vacunas candidatas como parte de una cartera diferenciada de vacunas para COVID-19», aseguró Ugur Sahin, CEO y cofundador de BioNTech. «Se han dado muchos pasos hacia este importante hito y nos gustaría dar las gracias a todos los involucrados por su extraordinario compromiso».